Na tropie zniszczonego kolagenu
Stworzone przed paroma laty przez naukowców z Uniwersytetu Johnsa Hopkinsa sztuczne białko po aktywowaniu ultrafioletem może skierować lekarzy do miejsc objętych chorobą, np. nowotworem czy zapaleniem stawów.
W artykule opublikowanym w PNAS (Proceedings of the National Academy of Sciences) akademicy pochwalili się, że ich białko pomyślnie przeszło testy na myszach, pozwalając zlokalizować raki prostaty i trzustki oraz nieprawidłowy wzrost kości w przebiegu zespołu Marfana.
Jak tłumaczą Amerykanie, sztuczna proteina nie obiera na cel chorych komórek, a zamiast tego wiąże się z pobliskim kolagenem, zniszczonym przez toczące się patologiczne procesy.
Kolagen to główne białko tkanki łącznej, które tworzy rusztowanie dla komórek budujących np. skórę czy kości. Pewne jego ilości są stale akumulowane/degradowane, jednak zmienione chorobowo komórki mogą wydzielać enzymy przyczyniające się do przyspieszonego rozkładu. Wynalazek z Uniwersytetu Johnsa Hopkinsa wykrywa właśnie miejsca nadmiernego remodelowania.
Chore komórki są jak złodzieje, którzy włamują się do czyjegoś domu i dokonują zniszczeń, ale pozostają nieuchwytni dla policji. Zamiast szukać włamywaczy, nasze białko reaguje na dowody pozostałe na miejscu zbrodni - tłumaczy S. Michael Yu.
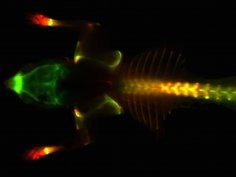
Podczas eksperymentów posłużono się peptydami naśladującymi kolagen (ang. collagen mimetic peptides, CMPs), które pod wpływem światła tworzą potrójną helisę i łączą się z kolagenem zdenaturowanym przez gorąco lub nadtrawionym przez metaloproteinazy macierzy zewnątrzkomórkowej. CMPs opatrzono znacznikami fluorescencyjnymi, dlatego miejsca związania białek można było wykryć dzięki mikroskopowi fluorescencyjnemu. Jest on podobny do mikroskopu optycznego, ale źródłem światła jest tu specjalna żarówka emitująca promieniowanie UV, np. lampa ksenonowa czy żarnik rtęciowy.
Kiedy w 2008 r. Michael Yu opowiadał o CMPs, dywagowano, że pewnego dnia będzie je można wykorzystać do szczegółowego obrazowania guzów czy płytek miażdżycowych w tętnicach, a także do poprawiania dopływu krwi do przeszczepionych tkanek. Teraz marzenia zespołu się spełniły, bo dzięki rozświetlonym obszarom zidentyfikowano położenie uszkodzonego kolagenu, a zatem i ogniska choroby.
Opracowując swoją technologię, Amerykanie napotkali na poważną przeszkodę. Zamiast ulegać hybrydyzacji ze zdegenerowanym kolagenem, CMPs łączą się bowiem ze sobą. Rozwiązaniem okazało się zastosowanie chemicznej klatki. Jest ona "rozbrajana" przez ultrafiolet tuż przed wprowadzeniem do krwioobiegu.
Podczas testów klatkowane CMPs wstrzyknięto myszom, u których występowały komórki ludzkiego raka prostaty i trzustki. W ciągu 4 dni wykonywano serię zdjęć. W ten sposób uwidoczniono rozprzestrzenianie się sztucznego białka za pośrednictwem naczyń oraz wyznakowanie miejsc, w których kolagen został uszkodzony przez procesy nowotworowe. Kolejne eksperymenty na zwierzętach zademonstrowały, że CMPs wiążą się ze zniszczonym kolagenem w kościach i chrząstce.




Komentarze (0)