Mikrobiom wpływa na przebieg chorób wywołanych genetycznie
Badania na myszach i ludziach pokazują, że mikrobiom jelit może wpływać na budowę naczyń krwionośnych w mózgu i odpowiadać za występowanie malformacji prowadzących do udaru bądź padaczki.
Publikacja, która ukazała się w piśmie Nature, zapewnia kolejne dowody dot. kwestii związków między bakteriami jelitowymi a zaburzeniami układu nerwowego.
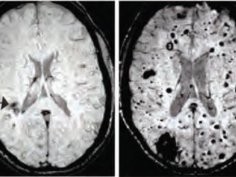
Naczyniaki jamiste ośrodkowego układu nerwowego (ang. cerebral cavernous malformations, CCMs) są skupiskami rozszerzonych, cienkościennych naczyń, które mogą prowadzić do drgawek lub udaru (gdy pojawia się krwawienie do otaczających tkanek).
Zespół z Uniwersytetu Pensylwanii badał mechanizmy CCM na zmodyfikowanych genetycznie myszach. Wtedy właśnie naukowcy natrafili na nieoczekiwane powiązania z mikrobiomem. Okazało się, że gdy wyeliminowano bakterie, liczba zmian znacząco się zmniejszyła.
Badanie jest fascynujące, bo pokazuje, że zmiany w organizmie mogą wpływać na postępy zaburzenia wywołanego przez mutację - podkreśla dr Jim I. Koenig z National Institute of Neurological Disorders and Stroke (NINDS).
Amerykanie prowadzili badania na modelu mysim, u którego po wstrzyknięciu leku wywołującego delecję genu rozwija się znacząca liczba CCMs. Okazało się jednak, że gdy zwierzęta przenoszono do nowego pomieszczenia, częstość pojawiania się CCMs spadła niemal do zera.
To była prawdziwa tajemnica. Nagle nasz niezawodny mysi model przestał wytwarzać zmiany, których się spodziewaliśmy. Co ciekawe, zmienność w tworzeniu naczyniaków występuje także u ludzi, ponieważ pacjentów z tą samą mutacją cechuje dramatycznie różny przebieg choroby - opowiada prof. Mark L. Kahn z Uniwersytetu Pensylwanii.
Dociekając, co się stało z myszami po przeprowadzce, student Kahna Alan Tang zauważył, że u tych nielicznych gryzoni, u których nadal rozwijały się CCMs, na brzuchach pojawiły się bakteryjne ropnie (są to zakażenia wywołane najprawdopodobniej wykonywanymi tu zastrzykami). W ropniach znajdowały się bakterie Gram-ujemne. Gdy podobne infekcje wywoływano celowo, u około połowy myszy rozwinęła się znacząca liczba CCMs.
Myszy, u których tworzyły się CCMs, miały też ropnie na śledzionie, co oznacza, że z pierwotnego miejsca zakażenia bakterie dostały się do krwiobiegu. To sugeruje związek między rozprzestrzenieniem bakterii konkretnego typu za pośrednictwem krwi i powstawaniem naczyniaków w mózgu - wyjaśnia Tang.
Jak w takim razie bakterie mogą wpływać na zachowanie naczyń w mózgu? Bakterie Gram-ujemne wytwarzają lipopolisacharyd (LPS), endotoksynę stanowiącą integralny składnik ich zewnętrznej błony komórkowej. Kiedy myszom robiono zastrzyki z LPS, wytwarzały liczne, duże CCMs. Gdy jednak genetycznie wyeliminowano receptor lipopolisacharydu TLR4, u myszy nie powstawały już naczyniaki. Naukowcy odkryli także, że u ludzi mutacje zwiększające ekspresję TLR4 również wiążą się z wyższym ryzykiem CCMs.
Wiedzieliśmy już, że tworzenie zmian w naczyniach mózgu może być napędzane przez bakterie Gram-ujemne za pośrednictwem sygnalizacji LPS. Kolejnym pytaniem było, czy można zapobiec CCMs, zmieniając mikrobiom - opowiada Kahn. Dalsze badania prowadzono na 2 sposoby: 1) noworodki myszy hodowano w sterylnych lub zwykłych warunkach, 2) myszy poddawano antybiotykoterapii, by zresetować ich mikrobiom.
U myszy wzrastających w sterylnych warunkach i przeleczonych antybiotykami liczba naczyniaków była znacząco mniejsza, co wskazało, że na tworzenie CCMs wpływa zarówno jakość, jak i liczebność mikrobiomu.
Kiedy zespół zastosował lek blokujący TLR4, liczba naczyniaków także znacząco spadła. Lek zastosowany do blokowania TLR4 testowano już na pacjentach z innymi schorzeniami. Niewykluczone, że sprawdzi się także w terapii CCMs, ale najpierw trzeba jeszcze wykonać sporo badań - zaznacza Kahn.
Wiedząc, że pacjenci z tą samą mutacją różnią się pod względem liczby i rozmiarów CCMs, Amerykanie chcą sprawdzić, czy zjawisko to da się wyjaśnić za pomocą ich mikrobiomów.




Komentarze (0)